3月3日,基因治疗公司uniqure(nasdaq: qure)宣布,公司收到了美国食品和药物管理局(fda)关于2026年1月30日举行的type a会议的最终会议纪要,会议讨论了一款治疗亨廷顿氏病(hd)aav基因疗法amt-130。

fda表示,与外部对照相比,i/ii期的研究数据不足以支持amt-130上市申请所需的有效性的主要证据。fda强烈建议uniqure开展一项前瞻性、随机、双盲、伪手术对照研究。uniqure计划继续与fda就3期开发的考虑进行沟通,并计划要求在2026年第二季度召开b类会议,进一步讨论潜在的研究设计方法。
uniqure首席执行官matt kapusta表示,虽然我们没有就基于第一/第二阶段数据的提交路径达成一致,但我们相信,我们数据的全面性和持久性保证了继续进行实质性对话,讨论fda对监管灵活性的承诺如何在这种情况下适当应用。我们仍然致力于与fda合作,为amt-130确定一条清晰、科学、有效的发展道路。
受此消息的影响,公司股价重挫33%,目前市值6.54亿美元。
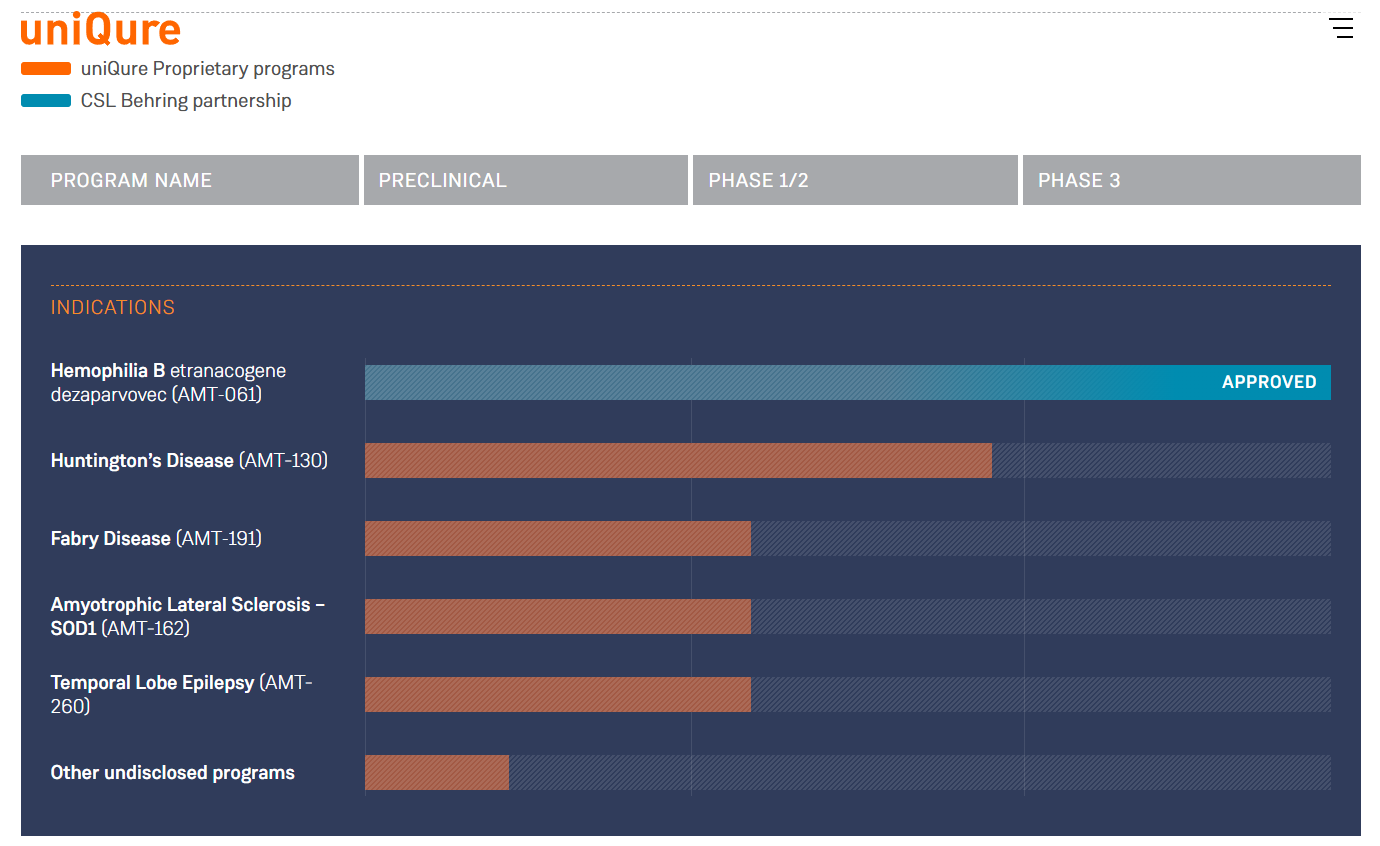
关于amt-130
amt-130由aav5载体组成,载体携带人工mirna,专门用于沉默亨廷顿基因,利用公司专有的miqure™沉默技术。治疗的目标是抑制突变蛋白(mhtt)的产生。利用aav载体将人工mirna直接传递到大脑,非选择性地敲低亨廷顿蛋白基因,这是治疗亨廷顿病的一种极具创新性和前景的方法。
关于i/ii期临床结果
参考资料:
公司米乐m6平台官网
米乐体育官方的版权声明:本文转自细胞基因治疗前沿,如不希望被转载的媒体或个人可与我们联系,我们将立即删除