药融圈监测显示:2024年8月底,刚成立半年的pre-merger oruka与美国纳斯达克上市公司arca biopharma完成反向并购,这家“空白壳”公司真正注入了资产与灵魂,交易完成后,存续主体沿用了oruka therapeutics。
公司不做“first-in-target”的高风险探索,而是把“抗体工程 半衰期延长”用在已验证的靶点上,靠给药频次和疗效优势取胜。
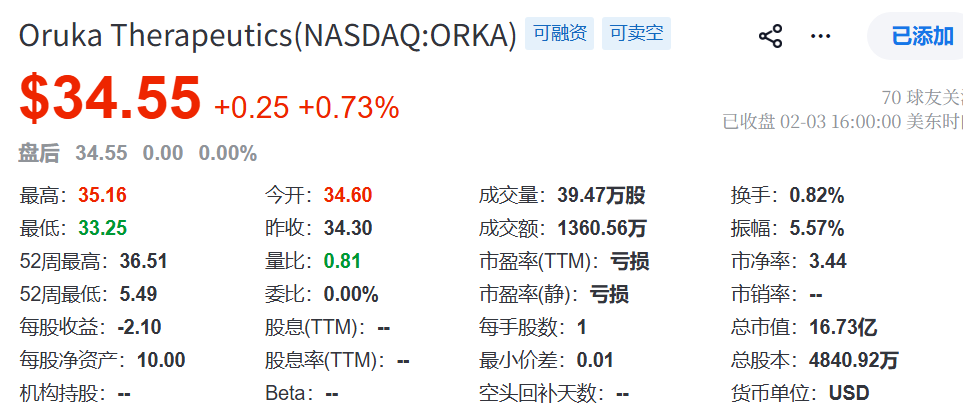
oruka的核心技术源自生物技术公司孵化巨头paragon therapeutics的yte(m252y/s254t/t256 e)突变fc平台。该突变在ph 6.0下增强与fcrn结合,可延长igg半衰期2~4倍,已在赛诺菲的dupixent、阿斯利康的synagis等药物上验证安全性和成药性。
oruka在此基础上做两件事:(1)把已验证的炎症靶点(il-23p19、il-17a/f)嫁接到yte骨架,降低靶点失败风险;(2)利用超高暴露窗口(cmax↑、auc↑)探索免疫重置——通过持续饱和占有il-23/il-17受体,耗竭皮肤驻留记忆t细胞,实现停药后6~12个月不复发。

公司把这一策略概括为“knockout”:用抗体暴露量击倒致病环路,而不仅是控制症状。基于此策略,目前研发管线情况如上。
orka-001是oruka therapeutics的first-in-class靶向il-23p19的抑制剂,也是公司超长半衰期和已验证靶点技术路线最直观的临床验证。
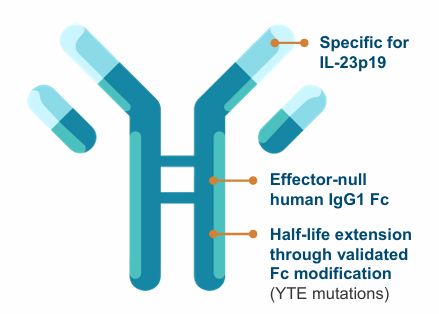
il-23是驱动银屑病等自身免疫性疾病的关键促炎细胞因子,由p19与p40两个亚基组成,p19仅存在于il-23,而p40还与il-12共享。orka-001特异性结合il-23的p19亚基,可以避免影响il-12的正常生理功能,在提升疗效的同时降低脱靶风险,安全性与现有il-23p19抑制剂类药物一致;orka-001通过fc段yte突变修饰,与新生儿fc受体(fcrn)的ph依赖性结合增强,体内半衰期延长至约100天,是同类药物瑞莎珠单抗(skyrizi)的3倍以上。高生物利用度带来持续的靶标抑制,为每年1~2次的超低给药频率奠定了基础;高浓度的il-23p19抑制可耗竭皮肤中的致病性组织驻留记忆t细胞(trm),实现免疫重置,有望让部分患者获得长期停药缓解,突破传统治疗仅能控制症状的局限。
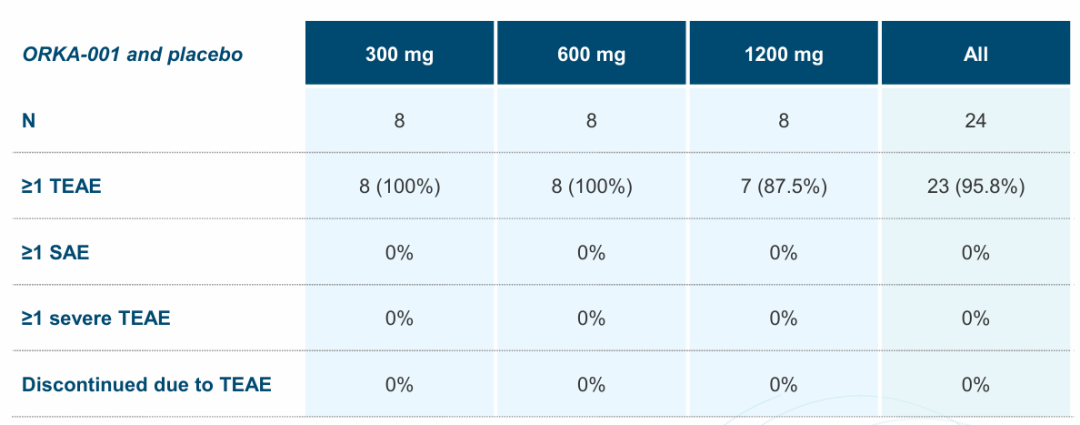
oruka在2024年第四季度启动了orka-001的临床试验1期研究,并在2025年9月公布了中期结果。该研究结果显示,orka-001的半衰期约为100天;单次剂量的orka-001在体外实验中显示能够完全且持续抑制stat3信号,这是一种il-23活性的下游标志,观察时间持续到24周;orka-001在所有剂量水平上均耐受良好,安全性特征良好,与抗il-23药物类别一致。
2025年第三季度,oruka启动了orka-001在中重度银屑病(pso)患者中的临床试验2a期研究(everlast-a试验),还计划在2026年上半年启动针对中重度银屑病患者的临床试验2b期剂量探索研究(everlast-b试验)。
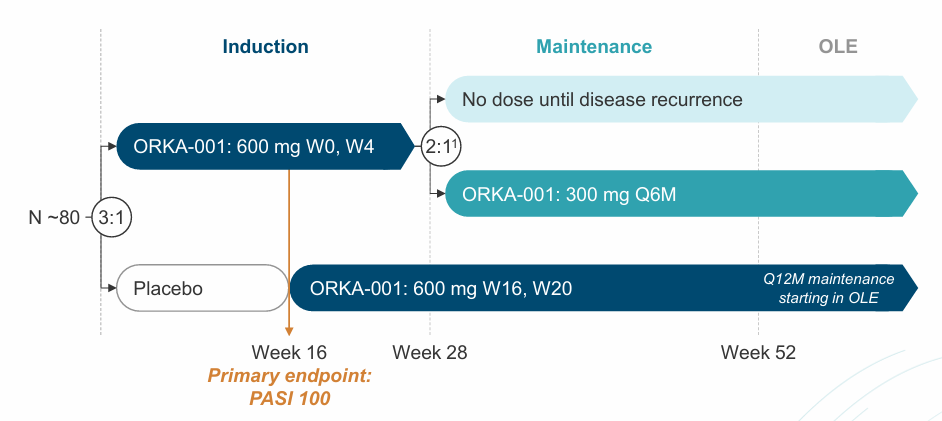
其中,everlast-a试验预计招募约80名患者,按3:1随机分配接受600毫克orka-001(第0周和第4周)或匹配安慰剂,主要终点为第16周pasi 100;第28周,已达到pasi 100的患者将按2:1随机分入两组,其中一组在疾病复发前不再接受另一剂量,以评估每年给药和延长期停止治疗的可能性,另一组每六个月接受一次orka-001(300mg)给药。预计在2026年下半年分享该研究的疗效和反应持续时间数据
注:pasi为银屑病面积及严重程度指数,pasi 100意味完全清除银屑病斑块
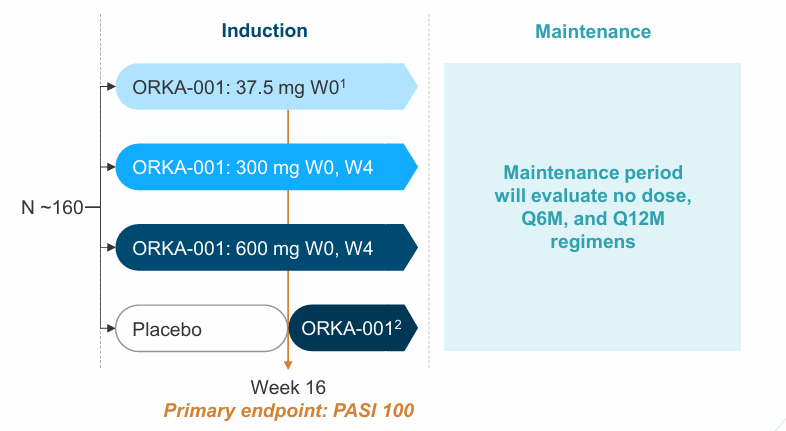
everlast-b试验将评估orka-001的三种剂量水平,分别是第0周37.5mg,第0周和第4周300mg,以及第0周和第4周600mg与安慰剂进行比较。主要终点是第16周pasi 100。为了加快开发,预计everlast-b的给药将在everlast-a完成之前开始招募患者。
orka-002是针对银屑病、银屑病关节炎等炎症性疾病开发的 il-17a/f双靶点抑制剂,其作用机制聚焦双靶点协同抑制。
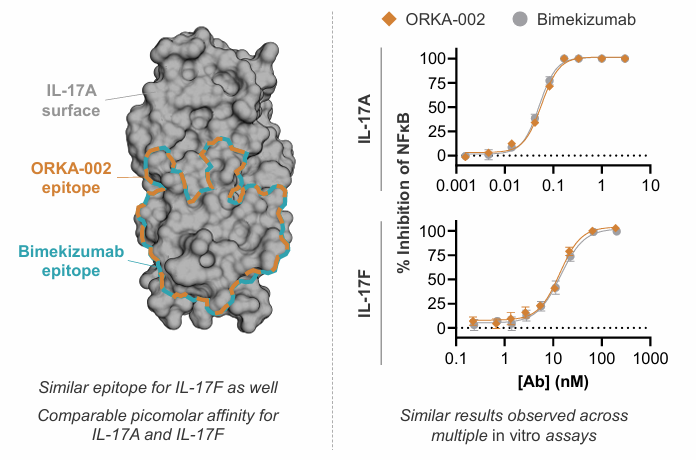
il-17a与il-17f同属il-17家族,同源二聚体或异源二聚体(a/a、f/f、a/f)均可激活il-17ra/rc复合物,驱动角质形成细胞释放cxcl1/3、il-36等炎症因子。临床已证明,特异性结合il-17a和il-17f两个炎症关键靶点,通过阻断这两种促炎细胞因子与受体的结合,抑制下游炎症信号通路激活,从源头减少炎症介质释放,缓解皮肤损伤和关节炎症。相较于单一il-17a抑制剂,il-17a/f双靶点抑制能覆盖更广泛的炎症场景,对部分单一靶点抑制剂应答不佳的患者可能更有效。
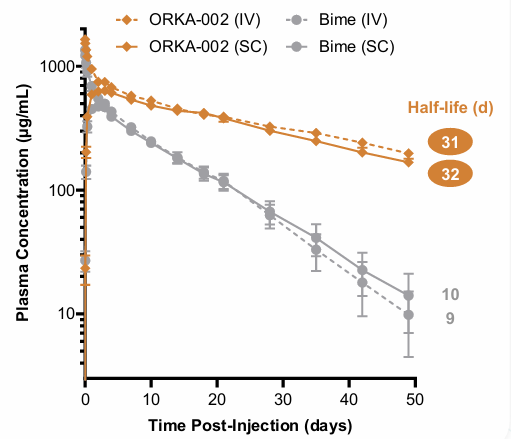
orka-002采用fc段优化技术延长半衰期,在食蟹猴体内半衰期达到同类药物比奇珠单抗(bimzelx)的3倍以上,预计人体半衰期可达50~75天。长效药代动力学特性支持每4~6个月给药一次,大幅优于现有il-17类药物每8周的给药频率,大幅提升了患者用药便利性。
其结合表位与比奇珠单抗高度相似,对il-17a/f的抑制活性达到皮摩尔级亲和力,在体外实验中展现出与同类药物相当的靶点结合能力和炎症抑制效果,同时避免对其他细胞因子通路的干扰,安全性与现有il-17抑制剂类药物一致。
注:bimzelx是首个通过选择性抑制il-17a和il-17f起效的银屑病治疗药物,目前临床开发中的其他il-17a/f抗体只有sonelokimab。
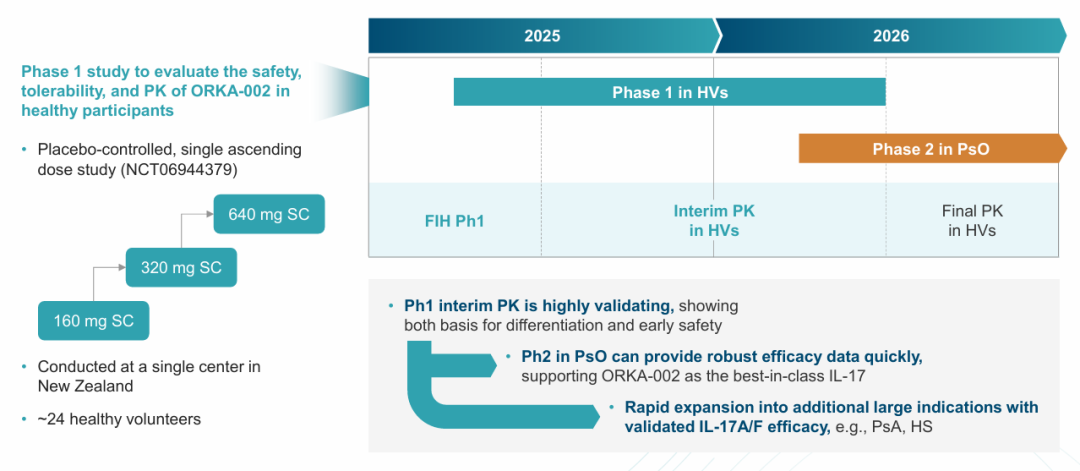
orka-002的临床试验1期研究旨在评估orka-002在健康受试者中的安全性、耐受性和药代动力学,2025年第二季度开始给药,目前已完成了160~640 mg单剂量爬坡试验,中期药代动力学证实了50~75天半衰期。预计在2025年年底分享中期数据,包括初步药代动力学数据,计划2026年上半年启动临床试验2期研究。
按照当前计划,orka-002后续可能会扩展到其他经过验证对il-17a/f有疗效的大型适应症,例如银屑病关节炎(psa)、化脓性汗腺炎(hs)等。
oruka认为orka-002与orka-001高度互补。对于仅表现为皮肤症状的中重度pso患者,最常使用il-23抑制剂进行治疗,因为这种机制治疗效果高且耐受性好;然而,对于伴有关节受累或psa(银屑病关节炎)体征和症状的患者,通常使用il-17抑制剂,因为它在改善皮肤和关节症状方面疗效显著;此外,对于皮肤症状高度顽固、使用il-23抑制剂治疗仍未充分缓解的患者,il-17抑制剂也常被采用。在此基础上,公司计划推进orka-002之后使用orka-001的序贯组合方案,即orka-021。
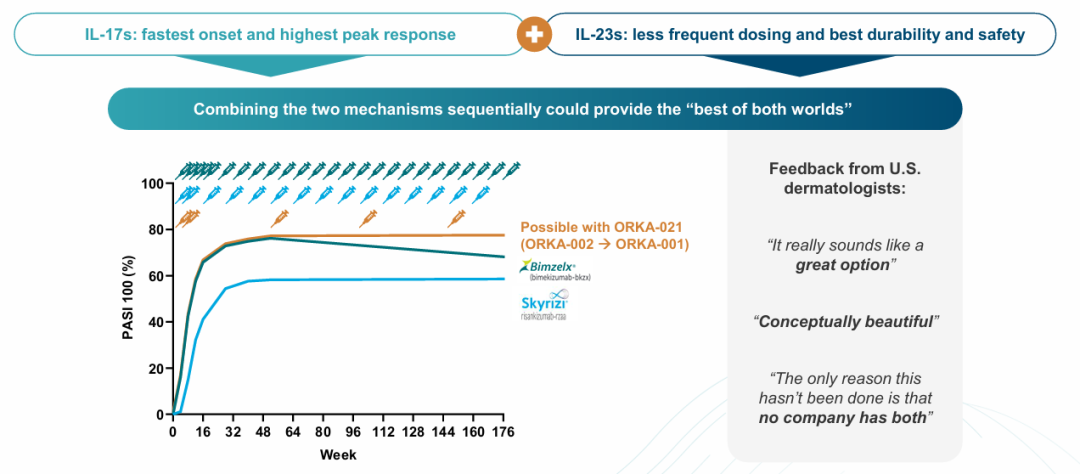
il-17a/f抑制剂的优势是起效快、峰值应答高,能快速清除皮损症状;il-23p19抑制剂则以长效性和安全性突出,可维持长期疾病控制,两者结合形成快速缓解和稳定维持的理想治疗曲线;il-17a/f和il-23均为银屑病炎症反应的核心驱动因子,前者直接介导皮肤炎症和组织损伤,后者调控致病性t细胞增殖分化。序贯抑制可从不同环节阻断炎症级联反应,既快速压制急性症状,又持续抑制慢性炎症复发,理论上比单一机制疗法更适用于中重度或难治性患者;依托两款单药的半衰期延长技术,orka-021的联合方案可简化给药频率,避免频繁注射,提升患者治疗依从性。
公司另一早期候选产品orka-003聚焦非il-23/17通路,用于扩展至特应性皮炎、斑秃等皮肤免疫疾病,预计2026年递交ind。
2025年前三季度,oruka总运营支出达8762万美元,较2024年同期(2024年2月成立至9月30日)的5781万美元增长52%,支出增长主要源于研发投入的扩大与运营规模的扩张。其中,研发支出7300万美元,占总支出的83.3%,一般及管理支出1462万美元,占总支出16.7%。
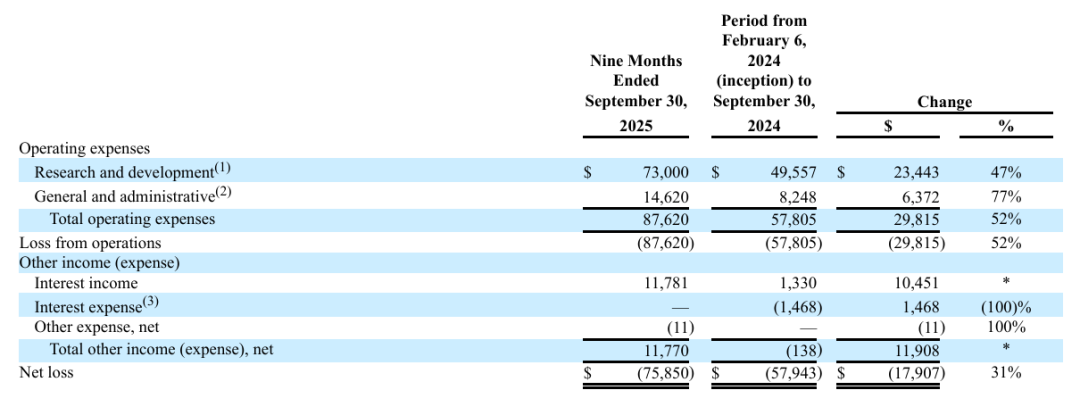
今年前三季度净亏损7585万美元,截至2025年9月30日,公司现金、现金等价物及有价证券合计5.009亿美元,其中现金及现金等价物9125万美元,有价证券4.10亿美元。