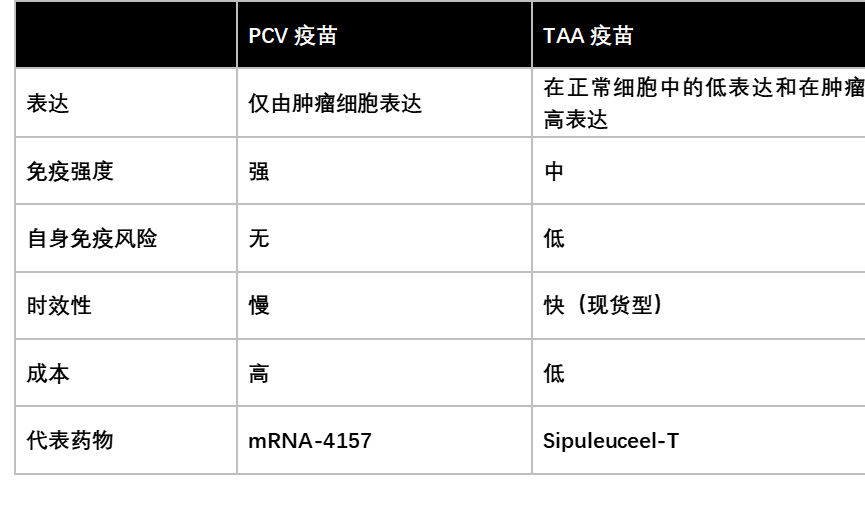
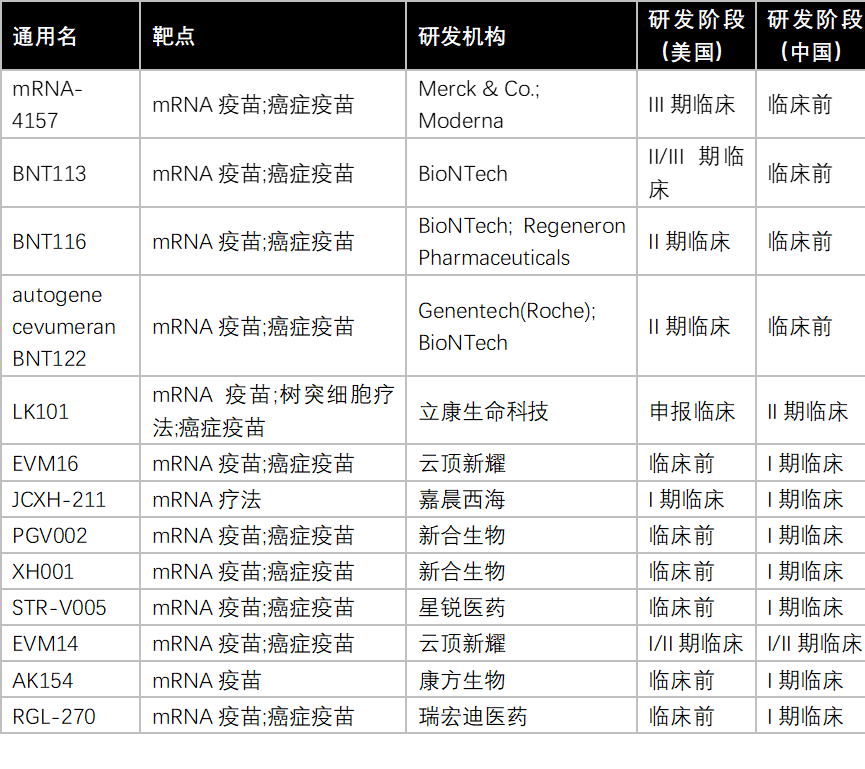
近年来,adc、多抗药物发展如火如荼。2024年,全球adc市场规模超130亿美元,最靓眼的两款药物仍属enhertu(37.5亿美元)和kadcyla(23.2亿美元);全球双抗药物市场规模达130亿美元,其中治疗血友病的hemlibra和治疗黄斑变性的vabysmo分别斩获53.6和44.1亿美元。新的技术路径是重磅药物诞生的摇篮,继adc、多抗后,治疗性癌症疫苗正浮出水面。近日,美国moderna公司和默沙东公司公布了癌症疫苗mrna-4157的2b期研究中位5年随访数据。在完全切除后的高危iii/iv期黑色素瘤患者中,mrna-4157联合pd-1抑制剂帕博利珠单抗(keytruda)的联合疗法,较keytruda单药治疗将复发或死亡风险显著降低49%。优异的疗效数据迅速转化为moderna股价的快速上行,短短两个月,moderna股价已然翻倍。肿瘤疫苗主要分为预防性肿瘤疫苗和治疗性肿瘤疫苗。预防性肿瘤疫苗已在市场上广泛使用,如用于宫颈癌防护的hpv疫苗。2023年,我国hpv疫苗市场规模达490亿元,其中九价疫苗市场规模近250亿元。尽管预防性肿瘤疫苗的市场规模近年来快速攀升,但治疗性肿瘤疫苗的研发却屡屡碰壁。究其原因,在于多数肿瘤治疗性疫苗在临床试验中难以显示出临床活性的确凿证据,疗效有限。肿瘤治疗性疫苗主要分为个体化新抗原疫苗(pcv)和肿瘤相关抗原疫苗(taa)。早期研究多针对肿瘤相关抗原(taa),其特征为在正常细胞中低表达及在肿瘤细胞中高表达,但由于抗原的泛表达性和免疫耐受性,疗效有限,目前仅sipuleuceel-t证实了其生存益处。个体化新抗原疫苗(pcv)是研究人员从肿瘤细胞中提取的与正常细胞不同的分子特征,可激活免疫系统定向清除癌细胞,因此可避免误伤正常组织,提升了药物的靶向性。此外,个体化新抗原疫苗可编码多种肿瘤抗原,通过将编码病毒蛋白的mrna递送至宿主细胞后快速表达目标蛋白,展现出更佳的治疗潜力,由默沙东和moderna联合研发的mrna-4157是其中的佼佼者。目前,sipuleucel-t和卡介苗是为数不多用于临床的肿瘤治疗性疫苗。(1)sipuleucel-t是一种由valeant pharmaceuticals公司研发的治疗性癌症疫苗,主要用于一线治疗无症状或症状轻微的转移性去势治疗无效的难治性前列腺癌(crpc)。sipuleucel-t于2010年4月获得美国fda批准,是迄今为止首个被fda批准的治疗性癌症疫苗。sipuleucel-t的上市基于一项三期研究,该试验入组512名受试者,按照2:1的比例随机分配至治疗组和安慰剂对照组。研究显示,接受sipuleucel-t的患者与安慰剂组中位生存期分别为25.8m和21.7m(hr=hr=0.78,p=0.03)。安全性方面,接受sipuleucel-t治疗的患者所报告的不良事件主要包括发冷、发热、头痛和感冒等,主要为1级和2级。丹瑞中国将sipuleucel-t引入中国,于2023年启动期关键性注册临床试验,截至目前已完成所有入组的140例患者的单采回输,进入临床观察期。其安全性和试验数据显示出积极的疗效和安全性结果,预计将于2026年递交上市许可申请(bla)。(2)卡介苗是用于预防肺结核病的疫苗,后发现对高风险非肌层浸润性膀胱癌(nmibc)有较好的疗效,进而在临床上广泛使用,目前是高风险非肌层浸润性膀胱癌局部病灶切除后的一线标准疗法。卡介苗可诱导局部免疫反应,将肿瘤细胞抑制灭除,减少局部复发和全身转移。但卡介苗存在膀胱刺激征、血尿和全身流感样症状等副作用。尽管有数款肿瘤疫苗上市,但目前尚未有mrna肿瘤治疗性疫苗登陆市场。与传统疫苗不同,mrna疫苗优势明显,一方面,mrna可在分裂细胞和非分裂细胞内翻译,rna只需进入胞质即可一步翻译成相关抗原,其蛋白质表达速率和幅度通常高于dna疫苗;另一方面,mrna疫苗不会整合到基因组序列中,因此不会引发插入突变。放眼全球,moderna和biontech在mrna疫苗的研发上崭露头角,其中备受关注的mrna疫苗包括mrna-4157和bnt116等。表:全球在研mrna肿瘤治疗性疫苗
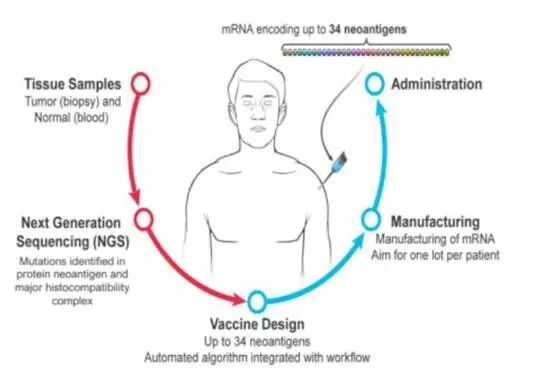
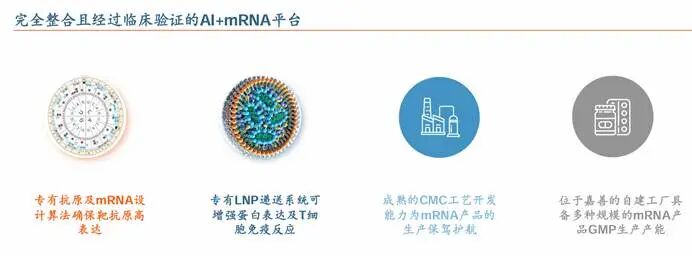
(1)mrna-4157是一款由默沙东(merck)和moderna联合研发的个体化新抗原mrna疫苗,旨在通过编码多达34种新抗原的合成mrna,根据每位患者肿瘤dna序列中的独特突变特性,量身打造特定的t细胞反应,从而激活抗肿瘤免疫反应。在2024年美国临床肿瘤学会(asco)年会上,moderna公布了mrna-4157(v940)联合帕博利珠单抗治疗完全切除后的高危ⅲ/ⅳ期黑色素瘤的ⅱb期研究的3年随访数据。与单独使用帕博利珠单抗相比,复发或死亡风险降低了49%,远处转移或死亡的风险降低了62%。mrna-4157(v940)联合帕博利珠单抗的2.5年无复发生存率为74.8%,而单独使用帕博利珠单抗的2.5年无复发生存率为55.6%。2026年1月,moderna披露了mrna个性化肿瘤疫苗mrna-4157联合pd-1抑制剂帕博利珠单抗的ⅱ期临床五年随访数据。结果显示,联合治疗组较单药组将患者复发或死亡风险显著降低49%。五年随访数据与三年持平,有力验证了mrna疫苗诱导持久免疫应答的科学假设。优异的数据令moderna和默沙东对mrna-4157充满信心。目前,mrna-4157有多项适应症处于注册性临床,包括黑色素瘤辅助治疗、皮肤鳞状细胞癌辅助治疗、非小细胞肺癌辅助治疗。moderna预计mrna-4157有望于2027年在美国上市,成为全球首个mrna治疗性疫苗。图:mrna-4157制备过程(2)bnt116是由biontech开发的一款mrna治疗性癌症疫苗,通过静脉注射的方式输入患者体内,bnt116由六种 mrna(cldn6、kk-lc-1、mage-a3、mage-a4、mage-c1 和 prame)组成,每种 mrna 都编码一种在非小细胞肺癌中经常表达的肿瘤相关抗原(taa)。bnt116旨在联合西米普利单抗(pd-1)治疗非小细胞肺癌。在2025年aacr大会上,biontech披露了一项名为luca-merit-1的1期试验,针对不适合接受一线化疗且pd-l1 tps≥1%的非小细胞肺癌患者,bnt116联合西米普利单抗orr达45%,mpfs达9.9m,三级及以上trae为15%。总的来看,bnt116 联合西米普利单抗在晚期非小细胞肺癌患者中表现出良好的抗肿瘤活性和可控的安全性。(3)bnt122是biontech与罗氏子公司genentech联合开发的一种基于尿苷信使 rna 脂质复合物(rna–lpx)的个性化新抗原特异性免疫疗法(inest)。每个分子编码多达10个新抗原,总共可编码多达20个新抗原。bnt122联合阿替利珠单抗和mfolfirinox化疗联用方案用于切除胰腺癌患者的辅助治疗展现出不俗的治疗潜力。ⅰ期研究结果显示bnt122联合阿替利珠单抗和mfolfirinox化疗联用方案在切除pdac患者中显著推迟了复发时间,诱导大量新抗原特异性、功能性和持久性的cd8 活性t细胞,并显示出良好的安全性。随着肿瘤治疗性疫苗的发展,国内企业纷纷加入这一赛道,多款产品处于临床ⅰ期,相关企业包括立康生命科技、云顶新耀、嘉晨西海、新合生物等。(1)lk101注射液是立康生命科技基于个体化肿瘤新生抗原设计的创新型疫苗。通过高通量测序和基于ai的肿瘤新生抗原分析,能够精准识别患者肿瘤细胞的特异性突变,并利用创新疫苗技术激活患者自身的免疫系统,精准攻击肿瘤细胞,达到治疗癌症的目的。2025年,lk101注射液获得美国食品药品监督管理局(fda)的ind(临床试验申请)批准,成为首个在fda获批的国产肿瘤新生抗原mrna疫苗产品。(2)evm16是云顶新耀自主研发的新型mrna个性化肿瘤治疗性疫苗。该疫苗的抗原由ai算法辅助完成开发。evm16已发表的一期研究免疫原性数据显示,新抗原总计检测率高达79.3%。2025年3月,evm16完成首例患者给药。云顶新耀预计将在未来6-12个月内将读出完整ia期临床数据,并随后启动ib期研究。图:云顶新耀自研的ai mrna平台(3)jcxh-211-iv是一款基于嘉晨西海新型自复制rna平台技术开发的first-in-class抗肿瘤免疫治疗药物,突破了传统il-12产品局部给药的限制。jcxh-211-it临床i期试验的中期数据已在asco2024会议上展示,jcxh-211-it表现出出色的安全性和耐受性以及显著的抗肿瘤生物活性。2024年7月5日,jcxh-211-iv获fda批准开展i/ii期临床。肿瘤治疗性mrna疫苗的研发曙光已现。mrna-4157凭借优异的临床数据,有望于2027年上市,成为全球首个肿瘤治疗性mrna疫苗。国内多家企业快速跟进,包括立康生命科技、云顶新耀、嘉晨西海、新合生物等。回首十年前,adc、双抗药物的发展可谓星星之火,弹指一挥间,已是超百亿美金的市场规模。十年后的今天,肿瘤治疗性疫苗即将冲破长夜,未来市场空间几何,我们且拭目以待。
米乐体育官方的版权声明:本文转自药事纵横,如不希望被转载的媒体或个人可与我们联系,我们将立即删除